质量摩尔浓度计算公式
摩尔浓度是一个用来描述一个溶液浓度的术语。它等于溶质的摩尔数(溶解的物质)除以千克的溶剂(溶解的物质)。摩尔浓度是不作为其相对浓度为常见但它采用的是非常具体的计算,尤其是涉及依数性(沸点升高,凝固点降低)。
| 质量摩尔浓度(m)= | 摩尔的溶质 |
| 溶液公斤 |
质量摩尔浓度公式例题:
1。如果1.57摩尔溶质溶于2.35公斤水溶液的摩尔浓度是多少?
答:
![]()
质量摩尔浓度(m)=0.668 摩尔
2. 如果124.2克NaOH氢氧化钠溶于1公升水溶液的摩尔浓度是多少?(水的密度等于 1.00 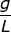 )
)
答:水被称为通用溶剂,密度通常被赋予 1.00 克/每升. 这使得从升到公斤的转换变得很容易.
在这个问题上 124.2 克的氢氧化钠需要转化成摩尔(摩尔溶质) 一公升的水需要转化成公斤。(千克的溶剂) 使用密度。
首先,求出摩尔质量 NaOH.
第二,换算克 NaOH为摩尔, 利用摩尔质量.
| 124.2克的NaOH = | 1摩尔的NaOH | = 3.105摩尔的NaOH |
| 40克的NaOH |
第三, 用密度把一公升的水转换成公斤。
| 1.0公升H2O | 1000mL | × | 1000g | × | 1公斤 | = 1.00公斤 |
| 1L | mL | 1000g |
最后, 用质量摩尔浓度方程求解。
| 质量摩尔浓度(m)= | 3.105摩尔的溶质 |
| 1.0公斤的H2O |
质量摩尔浓度(m)= 3.105molal
.
